|
|
|
发布时间: 2020-02-10 |
|
|
|
|
收稿日期: 2019-05-20
基金项目: 国家自然科学基金青年基金(51802190)
中图法分类号: O646
文献标识码: A
文章编号: 1006-4729(2020)01-0026-05
|
摘要
镍基催化剂作为碱性溶液中高催化活性和稳定的非贵金属催化剂, 广泛用于小分子电催化氧化领域研究。以磷掺杂碳纳米管为载体, 将负载镍/氧化镍核壳的纳米粒子用于甲醇小分子的电氧化, 获得了良好的稳定性及催化活性。在仅有3%的低负载量时, 在氧化峰电位, 其质量活性为6 800 mA/mg, 未掺杂碳纳米管载体上负载的纳米粒子活性仅为2 070 mA/mg。而且, 与CNTs相比, PCNTs为载体时甲醇电氧化的起始电位及氧化电位均有一定程度的负移。该高催化性能归因于镍/氧化镍核壳纳米粒子的小粒径, 以及磷掺杂碳纳米管载体与金属之间的相互作用。
关键词
磷掺杂; 碳纳米管; 甲醇电氧化; 载体; 催化剂; 相互作用
Abstract
Ni-based catalysts, as active and stable non-noble metal catalysts in alkaline solutions are widely used in the research of small molecule electrocatalytic oxidation.The Ni/NiO nanoparticles were anchoring on phosphorous doped carbon nanotubes for electrocatalytic methanol oxidation.Efficient catalytic activity and stability in electrocatalytic reaction were obtained.The NiO/Ni-PCNTs with a low nickel loading shows an mass activity of 6 800 mA mg-1at the peak potential of 3%, while that of its undoped counterpart is 2 070 mA mg-1.In addition both the onset and oxidation peak potentials of NiO/Ni-PCNTs for methanol oxidation shift negatively in comparison to CNTs.We proposed that the small particle size of Ni/NiO nanoparticles, and electronic effect arising from the interactions between PCNTs and Ni/NiO contribute to the improved electrocatalytic performances.
Key words
phosphorous doping; carbon nanotubes; electrocatalytic methanol oxidation; supports; catalysts; interaction
近年来, 具有结构和形态创新的纳米结构催化剂引起了广泛关注。在小分子电催化氧化过程中, 将铂(Pt)与其他金属(Fe, Co, Ni, Au等)合金化, 对Pt的壳层结构进行优化调整来构建高活性、高稳定性的电催化剂成为研究的热点[1-2]。通过调节Pt的电子结构, 即构建核壳结构减少贵金属Pt的用量, 以非Pt金属作为核, 利用核的晶格参数与贵金属的差异, 调节表面Pt壳的应力, 从而改变Pt与吸附物的结合强度, 提高催化活性; 而且, 中心核成分对Pt壳的表面原子层电子结构进行了调整, 能增强催化剂的催化活性和耐久性。另外, 调控合适的Pt壳层厚度可兼顾应变效应、减少Pt贵金属用量、稳定Pt层, 以及抑制非Pt金属的溶解。然而, 这些铂基核壳结构的合成过程往往涉及晶种诱导壳层生长、离子置换等复杂反应过程, 限制了此类催化剂的大规模生产和应用。镍基催化剂作为碱性溶液中高催化活性和稳定的非贵金属催化剂, 广泛用于小分子电催化氧化领域[3-5]。一般认为, 镍基催化剂中镍(Ni)的氧化还原电对(Ni2+/Ni3+)与未配对电子或空d轨道的氧化状态易于与小分子成键, 并发生反应。而且, 镍基催化剂可通过控制合成的温度气氛等条件, 形成稳定的氧化镍/镍核壳结构催化剂。
催化体系中使用的负载活性金属的载体是设计和合成催化剂时要考虑的重要因素。它不仅会影响电催化活性金属颗粒的大小、形态和分布, 而且会影响吸附和沉积过程中活性中间体的形成。未经修饰处理的原始碳材料表面化学性能通常处于惰性状态, 在催化剂制备过程中难以锚定金属粒子, 并且在催化反应中对反应物分子的吸附能力有限。未经处理的多孔碳载体对活性金属粒子的利用率较低, 而且催化反应过程在一定程度上增大了反应物和产物的传输阻力, 从而导致了催化效率低。金属粒子和原始碳材料在溶剂中的分散性不理想, 也会导致合成的催化剂难以在纳米尺度上具有高分散度, 活性金属粒子的团聚也会影响催化剂的活性。
非金属元素掺杂是修饰原始碳材料的一种有效方式。由于杂原子的键长、原子大小和电负性与碳原子有所差异, 掺杂到碳骨架中后会引入表面缺陷位置, 而且杂原子掺杂会引起原有碳表面电荷分布不均匀, 从而激发材料的电催化活性。掺杂有助于制备金属催化剂过程中金属粒子的成核, 并引起碳载体和金属颗粒之间的强界面相互作用。磷是一种5A族元素, 与氮具有相同的价电子数, 通常表现出相似的化学性质, 而且磷元素具有更高的电子给予能力, 表现出更强的N型(富电子)催化行为, 使其成为碳材料掺杂的广泛选择。碳材料, 如石墨层[6]、碳纳米管[7]和石墨烯[8]等, 经磷掺杂均表现出优异的电催化活性; 而且, 少量磷掺杂碳材料作为燃料电池中非金属催化剂时, 表现出良好的耐久性和高选择性。本文通过碳纳米管载体的磷掺杂, 引入磷官能团修饰碳表面, 调控镍金属纳米颗粒的粒径和分散度, 制备小粒径镍/氧化镍核壳结构催化剂, 并且通过金属与载体间的电子效应及相互作用力, 提高金属利用率, 优化小分子电催化反应动力学过程。实验结果表明, 该镍基核壳结构催化剂具有较高的电催化活性和稳定性。
1 催化剂的制备及表征
原始碳纳米管在高温管式炉中通入氢气/氦气气氛时, 通过NaH2PO2高温分解实现磷掺杂碳纳米管的制备。采用浸渍法制备磷掺杂碳纳米管负载镍/氧化镍颗粒。一定量的硝酸镍前驱体和磷掺杂碳纳米管均匀超声混合分散于溶剂中, 并搅拌至溶剂挥发完全, 将此产物烘干后, 于管式炉中氦气/氢气气氛中还原得到镍/氧化镍颗粒负载的磷掺杂碳纳米管催化剂。
图 1为镍/氧化镍颗粒在磷掺杂碳纳米管上的透射电镜(TEM)图和X射线能谱(EDX)图。由图 1(a)可以看到, 纳米颗粒粒径约为5 nm, 负载于磷掺杂碳纳米管上。由图 1(b)可看到, 碳、氧、磷、镍元素分布于碳纳米管上, 说明成功制备了Ni/NiO-PCNTs催化剂。
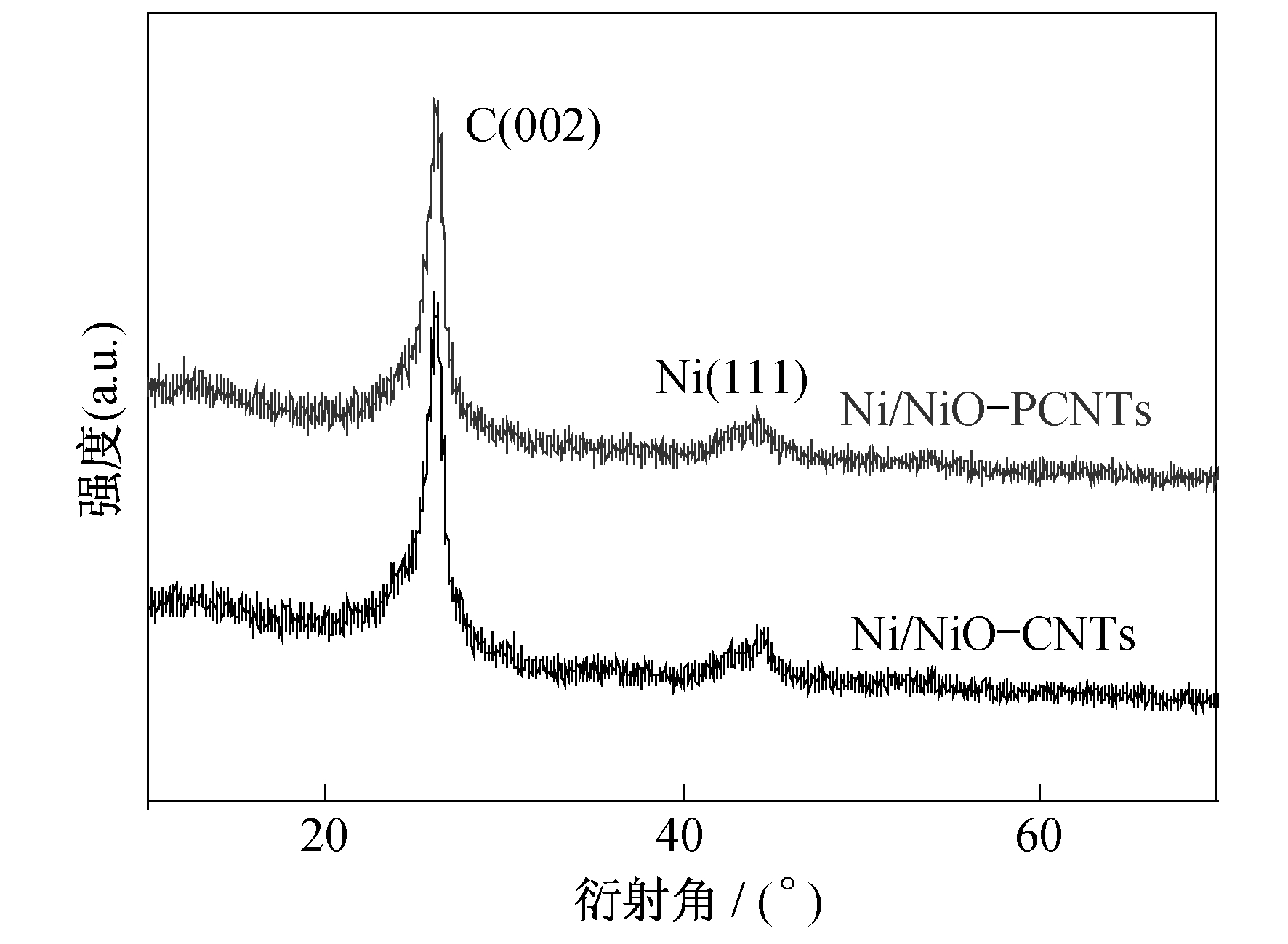
X射线衍射(XRD)通常用于对材料的物相分析。图 2为Ni/NiO-PCNTs和Ni/NiO-CNTs催化剂的XRD表征。由图 2可以看出, Ni(111)晶面及C的(002)晶面衍射峰均有出现, 然而没有出现NiO的衍射峰, 可能是由于NiO组分含量太少, 仅存在于催化剂核壳结构表面。
利用X射线光电子能谱(XPS)分析两种催化剂的表面化学性能, 结果如图 3和图 4所示。图 3对比了两种催化剂的Ni2p XPS图谱, 发现在磷掺杂碳纳米管的掺杂载体上Ni的Ni2p峰向低电子结合能方向移动, 说明载体与Ni/NiO之间存在金属-载体的相互作用, 而且发生了电荷转移。图 4所示的P2p XPS图谱显示, P通过两种键合方式掺杂到CNT中。133.8 eV时的峰值对应于P—O键, 132.1 eV时的峰值对应于P—C键。上述结果说明, 已成功在磷掺杂碳纳米管上负载了镍/氧化镍核壳结构小粒径纳米颗粒。
2 催化剂的电氧化性能
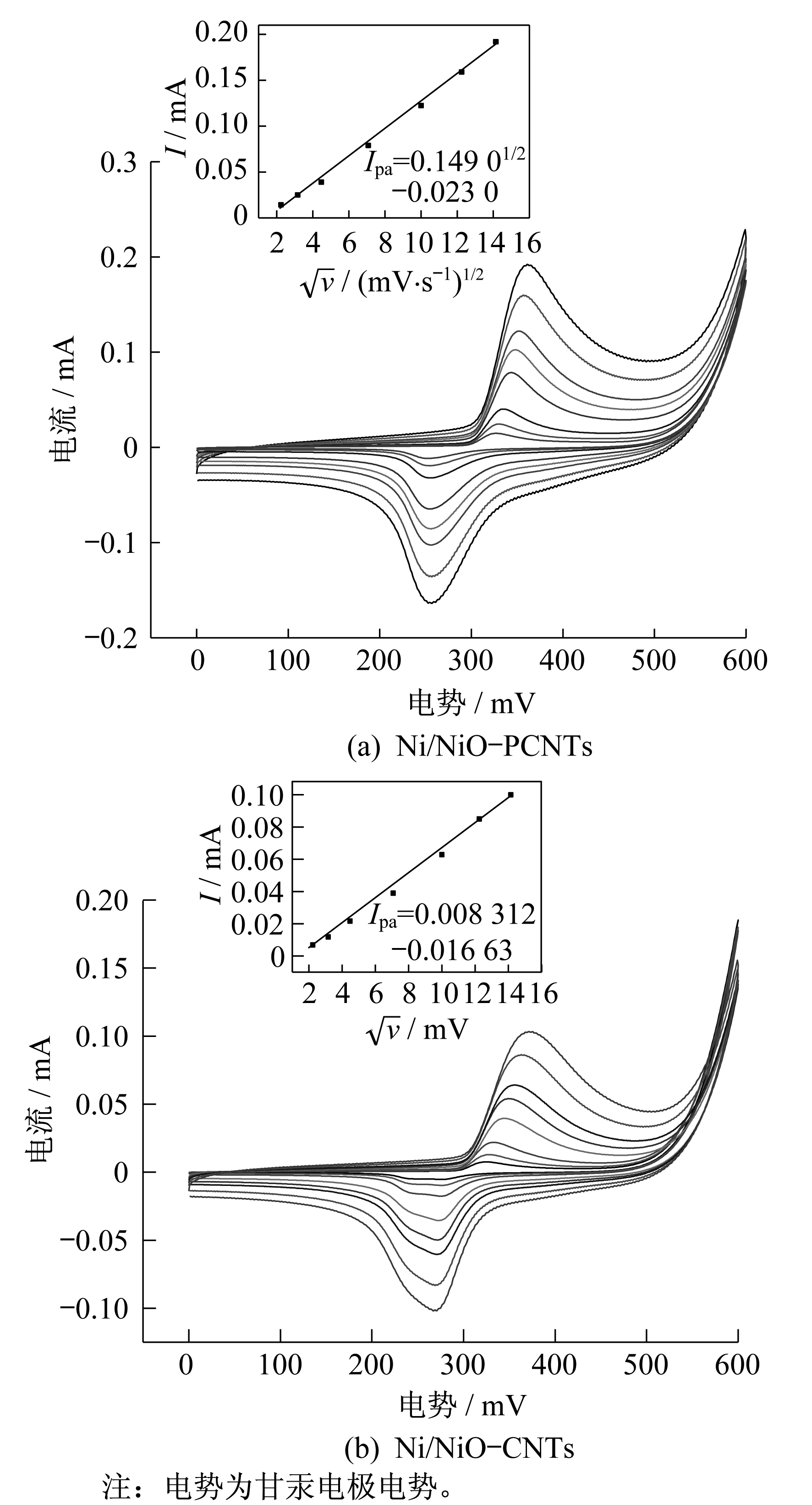
选取甲醇为目标小分子, 采用循环伏安法测定镍/氧化镍在载体上的电催化活性。Ni/NiO-PCNTs和Ni/NiO-CNTs两种催化剂在1.0 M(mol/L)KOH中的循环伏安曲线如图 5所示。在碱性介质中, 对甲醇氧化的电催化活性主要取决于Ni(OH)2/NiOOH的反应。图 5中, 可以在275 mV和360 mV左右观察到一对氧化还原峰, 这与Ni(II)/Ni(III)氧化还原对相对应。此外, 随着扫描速度的增加, 阳极峰电势正位移, 而阴极峰电势负位移。阳极和阴极峰值电流都随着扫描速率的增加而增加, 并且阳极峰值电流(IPA)与扫描速率平方根 之间存在线性关系。这表明Ni(OH)2/NiOOH的形成是一个受扩散控制的过程。从图 5(a)和图 5(b)的插图可以看出, NiO/Ni-PCNTs和NiO/Ni-CNTs的电流对应扫描数平方根的斜率分别为0.008 3和0.014 82。更大的斜率意味着OH-具有更高的扩散能力[9], 并且在NiO/Ni-PCNTs上可以形成比NiO/Ni-CNTs更多的电活性物质。
之间存在线性关系。这表明Ni(OH)2/NiOOH的形成是一个受扩散控制的过程。从图 5(a)和图 5(b)的插图可以看出, NiO/Ni-PCNTs和NiO/Ni-CNTs的电流对应扫描数平方根的斜率分别为0.008 3和0.014 82。更大的斜率意味着OH-具有更高的扩散能力[9], 并且在NiO/Ni-PCNTs上可以形成比NiO/Ni-CNTs更多的电活性物质。
氧化态镍物质中存在未配对的d电子或空d轨道, 可与被吸附的物质(如甲醇分子)或氧化还原中间体成键, 从而发生电氧化反应。
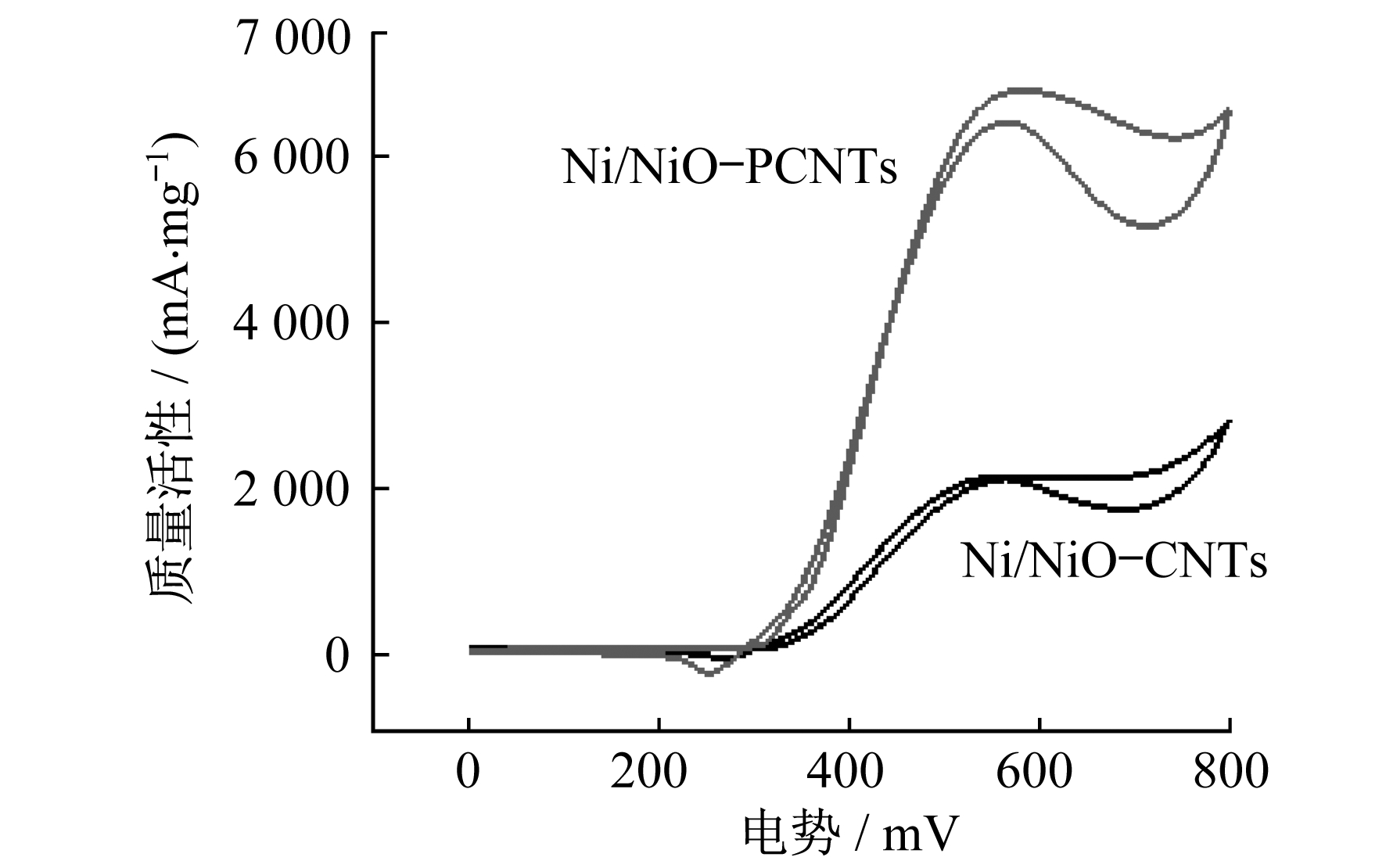
为了考察磷掺杂对催化剂活性的影响, 对甲醇氧化过程中的NiO/Ni-PCNTs和NiO/NiO-CNTs催化剂进行了CV测定。图 6为两种催化剂在1.0 M KOH+1.0 M CH3OH中的循环伏安曲线, 描述了在50 mV/s扫描速率下, 1M KOH/1M CH3OH溶液中两种催化剂的质量活性。与NiO/Ni-PCNTs(起始氧化电势为309 mV)相比, Ni/NiO-CNTs的起始氧化电势为284.4 mV, 该电位发生了负位移。在峰值电位下, NiO/Ni-PCNTs的质量活性(6 800 mA/mg)比NiO/NiO-CNTs(2 070 mA/mg)提高了3.28倍。
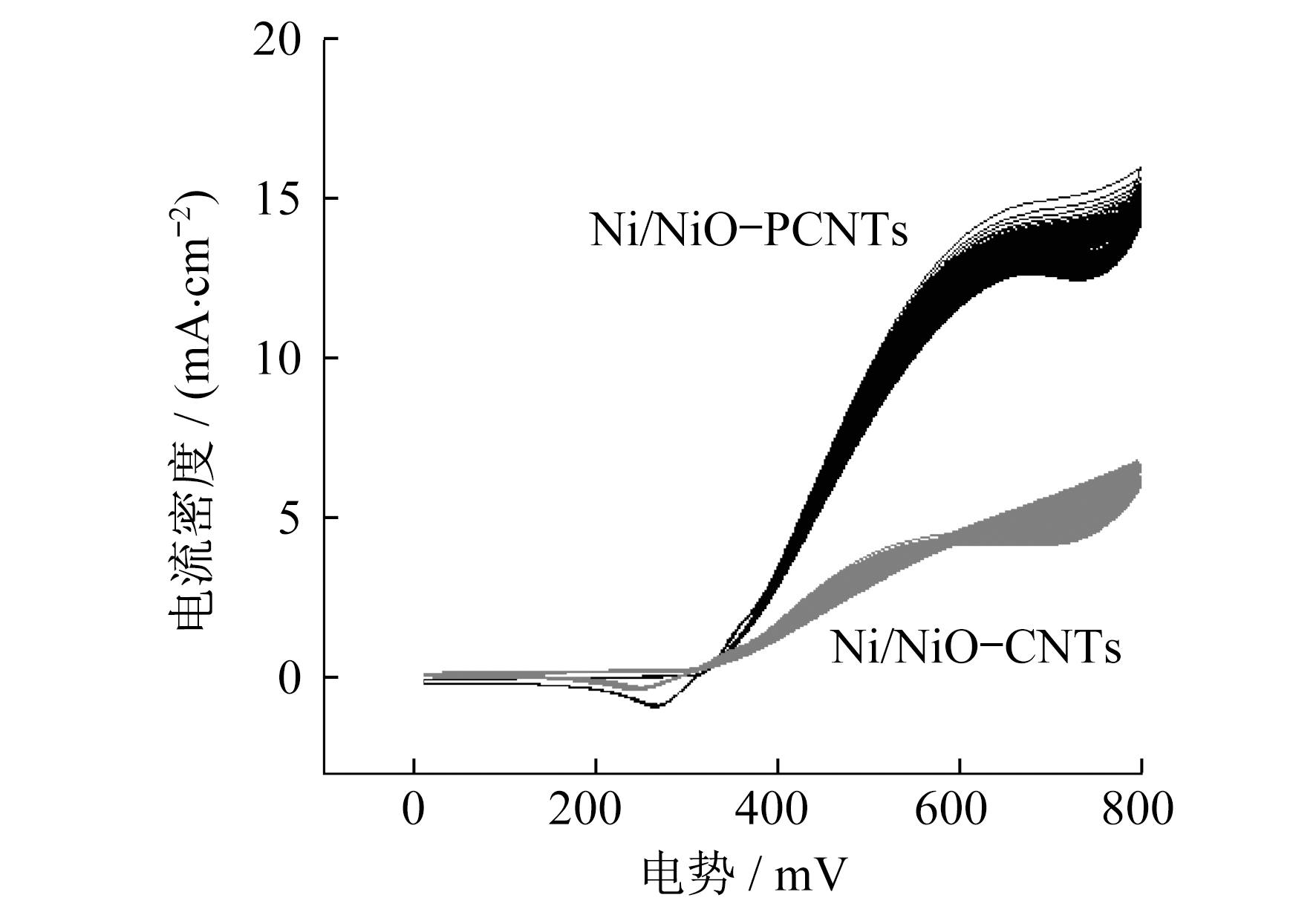
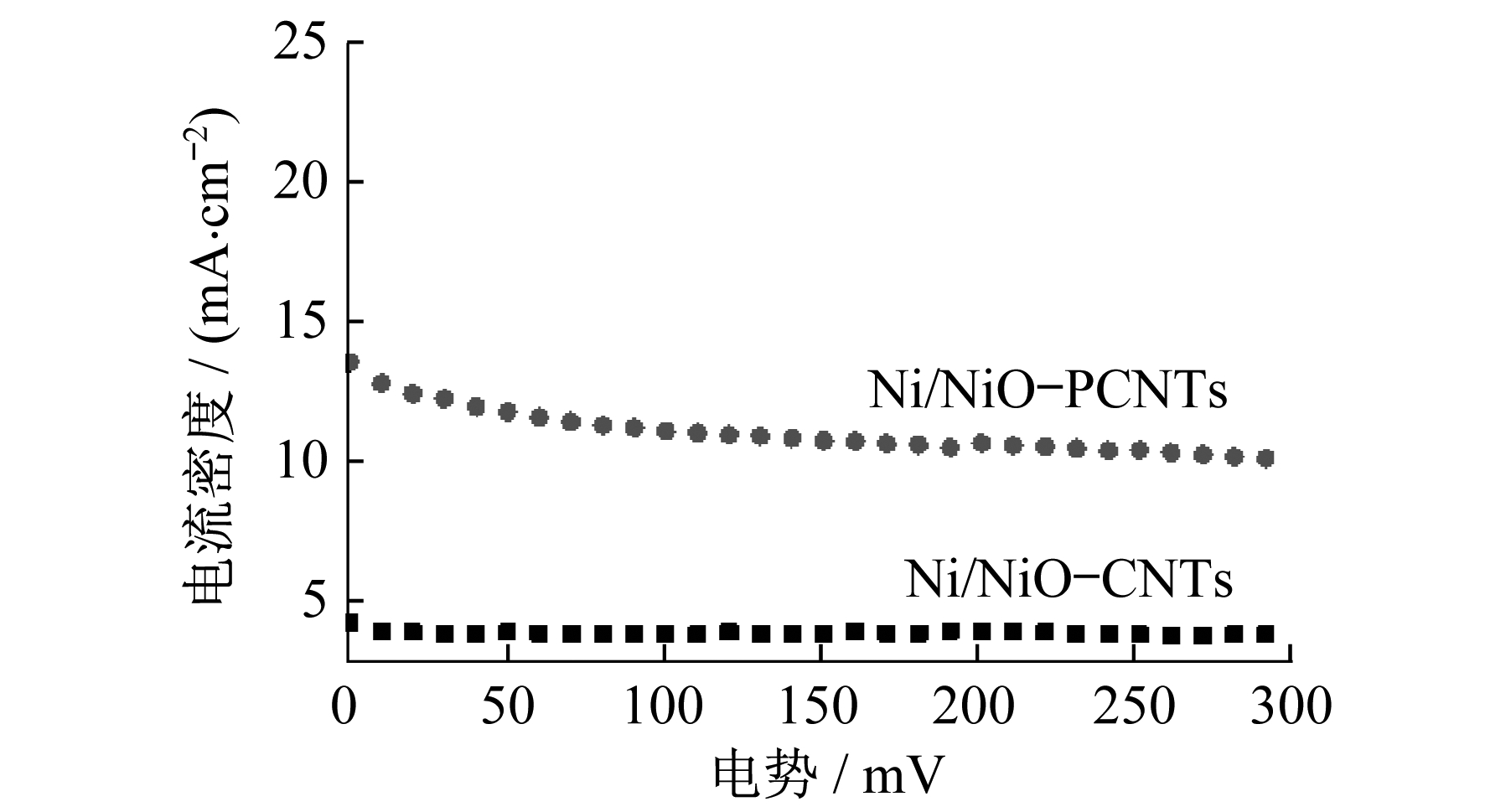
随着循环次数的增加, NiO/Ni-PCNTs和Ni/NiO-CNTs的循环伏安曲线见图 7。峰值电流密度的相应变化见图 8。图 7和图 8中电势均为其汞电极的电势。
由图 7和图 8可知, 经过50个循环后, 峰值电流密度随着循环次数的增加几乎稳定到300个循环, 与Ni/NiO-CNTs相比, Ni/Ni-PCNTs的催化活性和耐久性均较高。
经高温处理后, 磷掺杂主要以P—C和P—O键形式存在, 这说明含磷官能团成功掺杂到了碳骨架中。通过非金属元素磷掺杂, 能够在制备过程中为镍前驱体提供更多的锚定位点, 从而有利于镍/氧化镍颗粒的成核和生长。磷掺杂能够提高催化剂整体的导电性, 从而有利于在电催化氧化过程中电荷的传输, 提高反应速率。另外, 对比掺杂前后Ni的XPS峰位置, 发现Ni的结合能有一定程度上的负位移, 这说明磷掺杂改变了整个碳纳米管表面的电荷分布情况, 从而引起了金属镍和磷掺杂碳纳米管之间的相互作用, 它们之间的电子效应, 可能会促进电催化氧化反应的进行。
3 结语
本文以磷官能团化的碳纳米管作为锚定镍纳米颗粒的有效载体, 实现了高分散度Ni/NiO颗粒在载体上的有效负载。通过金属与载体间的电子效应及相互作用力, 提高了镍金属利用率。与未掺杂的Ni/NiO-CNTs相比, Ni/NiO-PCNTs具有更高的催化活性和稳定性。
参考文献
-
[1]KUTTIYIEL K A, SASAKI K, CHOI Y M, et al. Nitride stabilized PtNi core-shell nanocatalyst for high oxygen reduction activity[J]. Nano Lett, 2012, 12(12): 6266-6217. DOI:10.1021/nl303362s
-
[2]MIKKELSEN K, CASSIDY B, HOFSTETTER N, et al. Block copolymer templated synthesis of core-shell PtAu bimetallic nanocatalysts for the methanol oxidation reaction[J]. Chem Mater, 2014, 26(24): 6228-6940.
-
[3]SONG X, XI L, GUO Q, et al. CNT-Ni/SiC hierarchical nanostructures: preparation and their application in electrocatalytic oxidation of methanol[J]. Journal of Materials Chemistry A, 2013, 1(6): 2104-2109. DOI:10.1039/C2TA01002J
-
[4]ZHANG L, ZHAO J, LI M, et al. Preparation of graphene supported nickel nanoparticles and their application to methanol electrooxidation in alkaline medium[J]. New Journal of Chemistry, 2012, 36(4): 1108-1113. DOI:10.1039/c2nj20690k
-
[5]YI Q, HUANG W, ZHANG J, et al. Methanol oxidation on titanium-supported nano-scale Ni flakes[J]. Catalysis Communications, 2008, 9(10): 2053-2058. DOI:10.1016/j.catcom.2008.03.051
-
[6]LIU Z, PENG F, WANG H, et al. Phosphorus-doped graphite layers with high electrocatalytic activity for the O2 reduction in an alkaline medium[J]. Angewandte Chemie, 2011, 50(14): 3257-3261. DOI:10.1002/anie.201006768
-
[7]YU D, XUE Y, DAI L. Vertically aligned carbon nanotube arrays co-doped with phosphorus and nitrogen as efficient metal-free electrocatalysts for oxygen reduction[J]. J Phys Chem Lett, 2012, 3(19): 2863-2870. DOI:10.1021/jz3011833
-
[8]RAAMJOOEI F, SINGH K, SONG M, et al. Enhanced electrocatalytic activity due to additional phosphorous doping in nitrogen and sulfur-doped graphene: a comprehensive study[J]. Carbon, 2014(7): 257-267.
-
[9]KIM M, HWANG T, KIM K, et al. A study of the electrochemical redox behavior of electrochemically precipitated nickel hydroxides using electrochemical quartz crystal microbalance[J]. Journal of Electrochemical Society, 1997(5): 1537-1543.