|
|
|
发布时间: 2020-02-10 |
|
|
|
|
收稿日期: 2019-05-10
基金项目: 国家科技部国家重点研发计划“场地土壤污染成因与治理技术”重点专项(2018YFC1800600)
中图法分类号: X523
文献标识码: A
文章编号: 1006-4729(2020)01-0057-04
|
摘要
水滑石作为一种新型材料已广泛应用于医药、能源、环保等领域, 具有离子交换性、记忆效应、热稳定性、红外吸收性等特点。在水处理方面, 水滑石可以吸附难降解的有机物及无机离子, 去除率高且无二次污染。介绍了水滑石的合成方法及产物特点、水中无机离子和有机物的去除及其影响因素和水滑石的再生。
关键词
水滑石; 吸附; 离子交换; 再生
Abstract
As a new material, hydrotalcite has been widely used in medicine, energy, environmental protection and other fields.It is characterized by ion exchange, memory effect, thermal stability, infrared absorption and so on.In water treatment, refractory organic compounds and inorganic ions can be adsorbed by hydrotalcite with high removal rate and no secondary pollution.The synthetic method and product characteristics of hydrotalcite, the removal of inorganic ions and organic compounds in water, the influencing factors and the regeneration of hydrotalcite are introduced.
Key words
hydrotalcite; adsorption; ion exchange; regeneration
1 水滑石简介
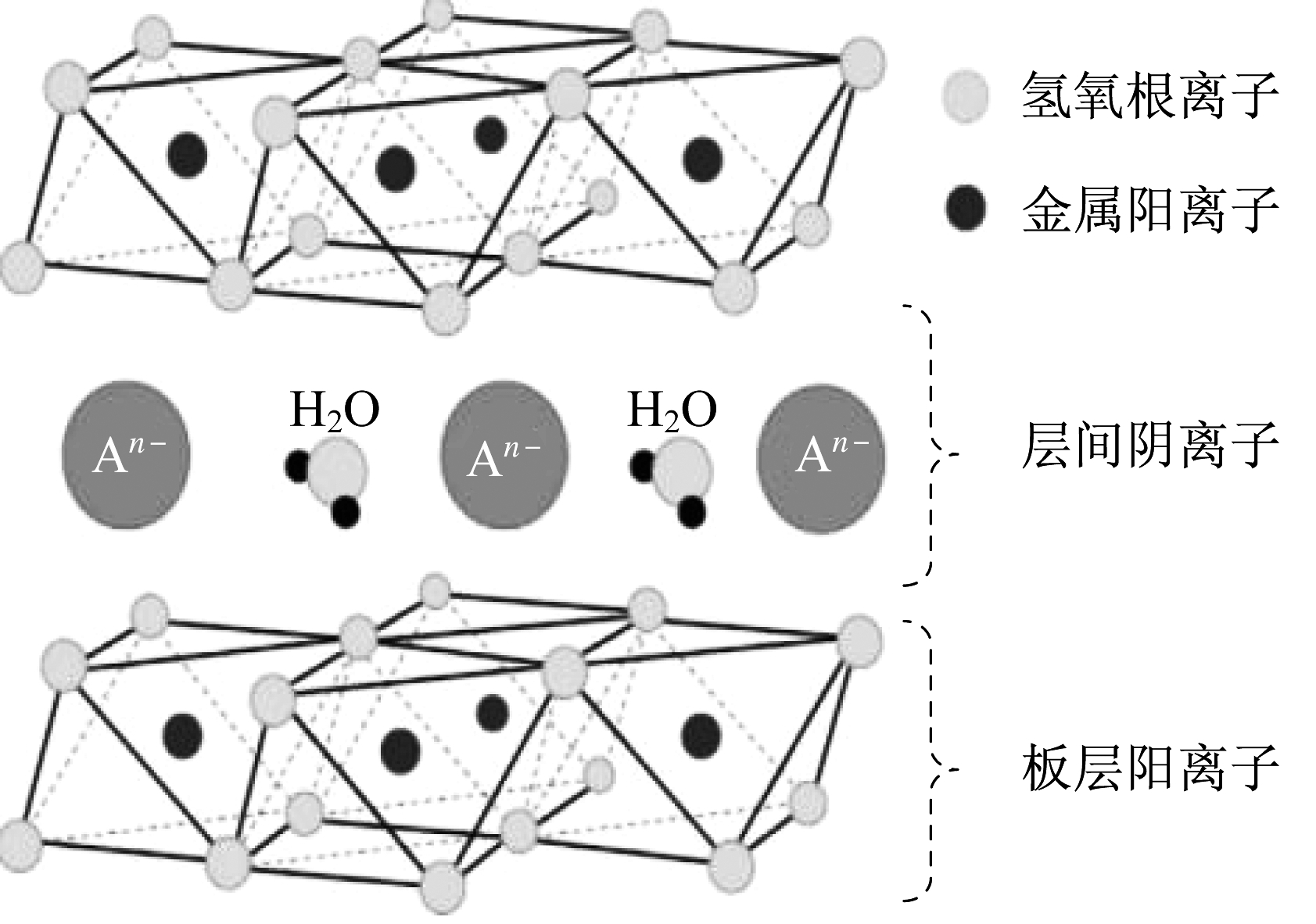
水滑石(Hydrotalcite)又称层状双金属氢氧化物(Layered Double Hydroxides, LDH), 是一种具有层状结构的阴离子黏土[1-3], 其结构与水镁石相似[3], 化学表达式为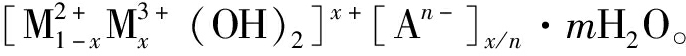 在这个表达式中, M2+和M3+分别表示二价和三价阳离子板层, 以共价键结合。An-表示层间可交换性阴离子, 以弱化学键(如离子键、氢键、静电力等)与主体层板相连[4], 使之具有离子交换的能力。其中
在这个表达式中, M2+和M3+分别表示二价和三价阳离子板层, 以共价键结合。An-表示层间可交换性阴离子, 以弱化学键(如离子键、氢键、静电力等)与主体层板相连[4], 使之具有离子交换的能力。其中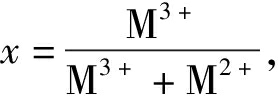 当
当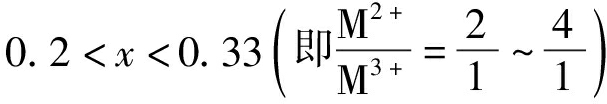 时, 水滑石结构趋于稳定[5]。当x过大, 板层的电荷密度过高会导致层间阴离子静电力加强, 使水滑石变得紧密[5]。水滑石具有层间阴离子交换性、记忆效应、热稳定性、红外吸收性能等特点[6], 不仅可以应用于污水的深度处理中, 而且在医药、汽油、纳米材料等行业中发挥了重要的作用[7-11]。在水处理过程中, 水滑石可以将一些难降解有机物及阴离子去除, 且无二次污染, 属于可再生资源。水滑石结构如图 1所示。
时, 水滑石结构趋于稳定[5]。当x过大, 板层的电荷密度过高会导致层间阴离子静电力加强, 使水滑石变得紧密[5]。水滑石具有层间阴离子交换性、记忆效应、热稳定性、红外吸收性能等特点[6], 不仅可以应用于污水的深度处理中, 而且在医药、汽油、纳米材料等行业中发挥了重要的作用[7-11]。在水处理过程中, 水滑石可以将一些难降解有机物及阴离子去除, 且无二次污染, 属于可再生资源。水滑石结构如图 1所示。
2 水滑石的合成方法
2.1 共沉淀法
共沉淀法[16]是将混合盐溶液和混合碱溶液按一定速度滴加到一定温度的蒸馏水中, 迅速搅拌, 滴定完毕后, 继续搅拌陈化, 最后经过滤、洗涤、烘干, 得到最终产物。此方法因其简单、价廉、产物稳定等特点而在实践中得到了广泛的应用。但该方法在共沉淀制备中存在着废水量大和资源浪费的问题。利用水滑石母液合成水滑石, 通过X射线衍射(XRD)进行表征, 发现其结晶度较好, 无多余杂质。这说明水滑石母液对水滑石的合成没有影响, 既节约了资源也提高了利用率。
2.2 水热法
2.3 焙烧复原法
焙烧复原法[16]则是利用其记忆效应根据水滑石母体组成成分选择一定的焙烧温度后放入到某种阴离子溶液中, 使其重新恢复成层状结构而制成最终产物。该方法容易生成非晶相物质, 且产物易受干燥条件、焙烧温度、焙烧时间、pH值等因素的影响。
2.4 成核/结晶隔离法
成核/结晶隔离法[16]是将混合盐溶液和混合碱溶液加入到全返混旋转液膜成核反应器中, 剧烈循环搅拌几分钟, 然后将浆液于一定温度下晶化而制成的。该方法具有产物稳定、晶体尺寸均匀等特点。
3 水滑石在水处理中的应用
3.1 阳离子的去除
3.2 阴离子的去除
3.3 有机物的去除
对于天然水中存在的有机物, 如腐殖酸、富里酸、微生物的代谢分泌物以及溶解的动植物组织等, 水滑石可作为预处理材料。天然水处理中, 腐殖酸与富里酸的初始浓度均为50 mg/L, 在pH=9.5及吸附温度为25 ℃时, 反应5 h, 水滑石对腐殖酸与富里酸的最大吸附量分别为105.2 mg/g和100.3 mg/g[23]。
4 水滑石在水处理中的影响因素
4.1 焙烧
焙烧会使水滑石失去层间阴离子和水, 比表面积增大、更易吸附溶液组分。通过扫描电子显微镜(SEM)对焙烧前后的水滑石进行表征发现, 各样品形貌变化不大, 仍然保持原有结构, 所以水滑石在焙烧中失去层间阴离子和水, 属于粒径不变的缩核反应模型[24]。在584 mg/L氯化钠溶液中投加焙烧前后的水滑石, 结果显示, 焙烧前水滑石经过3 h达到吸附平衡, 其最大吸附量为24.72 mg/g。焙烧后的水滑石在5 h达到平衡, 其最大吸附量是焙烧前的4倍, 为96.07 mg/g。在含有2 491.97 mg/L对苯二甲酸的工业废水中, 投加焙烧前后的水滑石, 结果显示, 焙烧后的水滑石吸附量是焙烧前的5.5倍, 其吸附量分别为475.13 mg/g和86.39 mg/g。
4.2 摩尔比
水滑石板层离子的摩尔比是影响水滑石吸附量的重要因素之一, 吸附量随着摩尔比的增大而逐渐增大。对于Mg-Al水滑石, 当摩尔比过小时, 水滑石结构中层板上的电荷密度过大, 对层间阴离子的作用力增加, 会导致层间距减小, 这不利于对溶液中离子的吸附; 而随着摩尔比的增加, 主体层板电荷密度减小, 对层间阴离子吸附作用力变弱, 导致层间距增大, 这将有利于层间阴离子的交换, 使得去除率相应得到提高[25]。在含有50 mg/L的氯离子溶液中投加Mg-Al水滑石后发现, 当n(Mg/Al)=4时去除率最大, 吸附量为10.75 mg/g。
4.3 pH值
水滑石对pH值有很强的缓冲能力。当pH值低时, 水滑石会部分溶解释放OH-离子使pH值升高; 当pH值高时, 水滑石会吸附水溶液中的OH-离子使其下降。水滑石类化合物在一定的pH值范围内, 对离子的吸附量保持稳定:当pH值高于一定值时, 会有大量OH-参与吸附竞争; 而当pH值低于一定值时, 又使水滑石部分溶解。这些都使水滑石的吸附容量减少。在处理含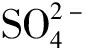 的废水时, 水滑石对
的废水时, 水滑石对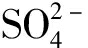 的吸附量随pH值的增加而下降; 当pH值分别为8, 10, 12时, 吸附量分别为45 mg/g, 40 mg/g, 20 mg/g; 在酸性环境下,
的吸附量随pH值的增加而下降; 当pH值分别为8, 10, 12时, 吸附量分别为45 mg/g, 40 mg/g, 20 mg/g; 在酸性环境下,
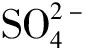 的吸附量随pH值的减小而下降; 当pH值为6和4时, 吸附量分别为35 mg/g和25 mg/g[26]。处理含氟废水时, 当反应300 min及pH=8时, 氟离子的吸附量为90 mg/g; 当pH=9时, 吸附量下降到20 mg/g[27]。
的吸附量随pH值的减小而下降; 当pH值为6和4时, 吸附量分别为35 mg/g和25 mg/g[26]。处理含氟废水时, 当反应300 min及pH=8时, 氟离子的吸附量为90 mg/g; 当pH=9时, 吸附量下降到20 mg/g[27]。
4.4 共存离子
4.5 水滑石剂量
随着水滑石剂量的增多, 其吸附能力受到的约束力增大。水滑石表面是非均相的, 其吸附容量与其表面活性位点有着密切联系。高剂量的水滑石, 由于其颗粒聚集度高, 高表面能位点减少而低表面能位点增加, 即有效表面积没有显著增加, 所以投加量增加到一定值后, 效果变化不大。实验表明, 在初始浓度为100 mg/L的硝酸盐溶液中, 随着Mg-Fe水滑石用量的增加,
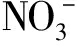 的去除率逐渐增大, 而吸附容量却随着水滑石剂量的增加而减小。当水滑石用量为1.5 g/L时, 吸附容量为90 mg/g; 当水滑石用量为2.5 g/L时, 吸附容量为40 mg/g[3]。
的去除率逐渐增大, 而吸附容量却随着水滑石剂量的增加而减小。当水滑石用量为1.5 g/L时, 吸附容量为90 mg/g; 当水滑石用量为2.5 g/L时, 吸附容量为40 mg/g[3]。
5 水滑石的再生
水滑石的再生是指利用水滑石的记忆效应, 通过焙烧的方式脱除层间离子再投加到再生液中恢复其原有结构。通常选用NaNO3, NaOH, Na2CO3, (NH4)2CO3, 或者是这些溶液中某两种溶液的混合溶液作为再生液[30]。对于不同类型的水滑石, 再生液对其再生性具有不同的影响。选用NaOH和NaCl再生Mg-Mn水滑石, 在150 mg/L的磷酸根溶液中, 室温下经过5 h后, 磷酸根吸附量分别为45 mg/L和55 mg/L, 表明NaCl比NaOH更适合Mg-Mn水滑石的再生[31]。Mg-AI-LDHs的再生选用Na2CO3溶液浸泡8~10 h, 在浓度为100 mg/L的氯离子溶液中, 室温下经过5 h后氯离子吸附量达到50 mg/g, 与再生前效果相同[32]。
6 结语
目前, 水滑石大量用于高浓盐废水的治理中, 尤其是氯离子和硝酸盐的去除。研究表明, 通过改变水滑石板层金属离子的种类和数量可以提高其吸附性能。有学者通过从废弃的材料中提取可再生利用的金属离子来合成水滑石。由于水滑石具有较高的机械强度、热稳定性和可再生性, 可作为催化剂载体用于催化剂再生。在水滑石合成方面, 连续生产工艺可以扩大层状金属氧化物的生产规模, 并避免了常规共沉淀的缺点, 未来将设计一体化合成装置进行大规模的生产。
参考文献
-
[1]硝酸根插层钴铝类水滑石的一步原位合成与表征[J]. 材料导报, 2017, 31(30): 201-204.
-
[2]阴离子黏土处理增强型地热系统返排液的研究[J]. 环境化学, 2018, 37(2): 335-346.
-
[3]徐盼.类水滑石的制备及其对水中硝酸盐的去除研究[D].广州: 华南理工大学, 2013.
-
[4]多酸插层水滑石复合材料的新进展[J]. 中国科学, 2017, 47(4): 451-464.
-
[5]EIBY S H J, TOBLERA D J, NEDEL S, et al. Competition between chloride and sulphate during the reformation of calcined hydrotalcite[J]. Applied Clay Science, 2016, 132: 650-659.
-
[6]乙二胺四乙酸根插层镁-铝水滑石的制备与性能[J]. 中国粉体技术, 2016, 22(2): 48-50.
-
[7]FAN G L, LI F, EVANS D G, et al. Catalytic applications of layered double hydroxides: recent advances and perspectives[J]. Royal Society of Chemistry, 2014, 43(20): 7040-7066. DOI:10.1039/C4CS00160E
-
[8]SIDRA I, VARSHA S, MIKA S. Synthesis and application of LDH intercalated cellulose nanocomposite for separation of rare earth elements(REEs)[J]. Chemical Engineering Journal, 2017, 309: 130-139. DOI:10.1016/j.cej.2016.10.028
-
[9]DAUD M, SHAHZAD K M, FARRUKH S. Graphene/layered double hydroxides nanocomposites: a review of recent progress in synthesis and applications[J]. Carbon, 2016, 104: 241-252. DOI:10.1016/j.carbon.2016.03.057
-
[10]CAO Y, LI G T, LI X B. Graphene/layered double hydroxide nanocomposite properties, synthesis, and applications[J]. Chemical Engineering Journal, 2016, 292: 207-223. DOI:10.1016/j.cej.2016.01.114
-
[11]ZHAO Y F, JIA X D, WATERHOUSE G I N. Layered double hydroxide nanostructured photocatalysts for renewable energy production[J]. Advanced Energy Materials, 2016, 6(6): 1-20.
-
[12]YANG Z Y, ZHOU H W, ZHANG J C, et al. Relationship between Al/Mg ratio and the stability of single-layer hydrotalcite[J]. Acta Physico Chimica Sinica, 2007, 23(6): 795-800. DOI:10.1016/S1872-1508(07)60045-X
-
[13]BASKARAN T, KUMARAVEL R, CHRISTOPHER J, et al. Silicate anion intercalated cobalt-aluminium hydrotalcite(CoAl-HT-Si): a potential catalyst for alcohol oxidation[J]. Royal Society of Chemistry, 2014, 4(22): 11188-11196.
-
[14]FAN G L, WANG H, XIANG X, et al. Co-Al mixed metal oxides/carbon nanotubes nanocomposite prepared via a precursor route and enhanced catalytic property[J]. Journal of Solid State Chemistry, 2013, 197: 14-22. DOI:10.1016/j.jssc.2012.08.016
-
[15]Zn-Al水滑石催化碳酸二甲酯与苯酚酯交换反应的研究[J]. 高等学校化学学报, 2005(8): 1502-1506. DOI:10.3321/j.issn:0251-0790.2005.08.024
-
[16]类水滑石化合物制备方法研究综述[J]. 南京师大学报(自然科学版), 2009, 32(2): 82-86.
-
[17]尿素法合成镁铁水滑石的制备机理[J]. 硅酸盐学报, 2011, 39(2): 365-370.
-
[18]镁铝铜水滑石的合成、表征及性能研究[J]. 材料科学与工程学报, 2003, 21(5): 717-720. DOI:10.3969/j.issn.1673-2812.2003.05.024
-
[19]李松南.磁性水滑石及其改性材料对六价铬及铜离子吸附性能的研究[D].哈尔滨: 哈尔滨工程大学, 2009.
-
[20]JIANG J Q, ASHEKUZZAMAN S M, HARGREAVES J S J, et al. Removal of Arsenic(III)from groundwater applying a reusable Mg-Fe-Cl layered double hydroxide[J]. Journal of Chemical Technology and Biotechnology, 2014, 90(6): 1160-1166.
-
[21]许昶雯.类水滑石同时去除水中氟离子和硬度吸附性能研究[D].太原: 太原理工大学, 2018.
-
[22]斜发沸石负载Mg-Al-Fe水滑石在处理含氯废水中的应用研究[J]. 硅酸盐通报, 2013, 32(12): 2481-2484.
-
[23]镁铝水滑石及焙烧产物去除水中的天然有机物[J]. 环境工程学报, 2014, 8(10): 4053-4059.
-
[24]不同形貌镁铝水滑石的可控合成及其对氯离子的吸附性能[J]. 精细化工, 2017, 34(10): 1107-1113.
-
[25]纳米水滑石的结构表征及其对氯离子的吸附性能[J]. 材料科学与工程学报, 2016, 34(6): 998-1003.
-
[26]类水滑石复合材料吸附去除水中硫酸根离子[J]. 环境科学, 2016, 37(3): 1000-1007.
-
[27]LIANG L, JING H, MIN W, et al. Treatment of high fluoride concentration water by Mg Al-CO3 layered double hydroxides: kinetic and equilibrium studies[J]. Water Research, 2007, 41: 1534-1542. DOI:10.1016/j.watres.2006.12.033
-
[28]KAMEDA T, YOSHIOKA T, MITSUHASHI T, et al. The simultaneous removal of calcium and chloride ions from calcium chloride solution using magnesium-aluminum oxide[J]. Water Research, 2003, 37: 4045-4050. DOI:10.1016/S0043-1354(03)00311-7
-
[29]AKINO T, MIHO U, AKITSUGU O. Synthesis and sulfate ion-exchange properties of a hydrotalcite-like compound intercalated by chloride ions[J]. Journal of Hazardous Materials, 2006, 143(1): 582-586.
-
[30]耿翠玉.焙烧水滑石前体合成方法对其选择性吸附含硫阴离子的影响及再生性能[D].北京: 北京化工大学, 2013.
-
[31]RAMESH C, SATOKO T, AKINARI S, et al. Adsorption of phosphate from seawater on calcined MgMn-layered double hydroxides[J]. Journal of Colloid and Interface Science, 2005, 290: 45-51. DOI:10.1016/j.jcis.2005.04.025
-
[32]胡静.焙烧镁铝碳酸根水滑石在含氯废水处理中的应用基础研究[D].杭州: 浙江大学, 2005.




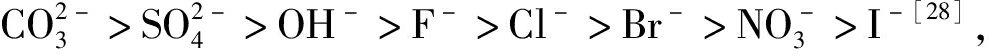 具有高电荷密度的阴离子会对板层呈现高的静电力。有学者提出增加层间的电荷密度有利于
具有高电荷密度的阴离子会对板层呈现高的静电力。有学者提出增加层间的电荷密度有利于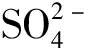 的去除[
的去除[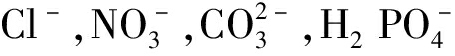 与
与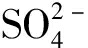 共存以及没有共存离子的情况下类水滑石复合材料吸附
共存以及没有共存离子的情况下类水滑石复合材料吸附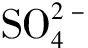 后的FT-IR谱图。
后的FT-IR谱图。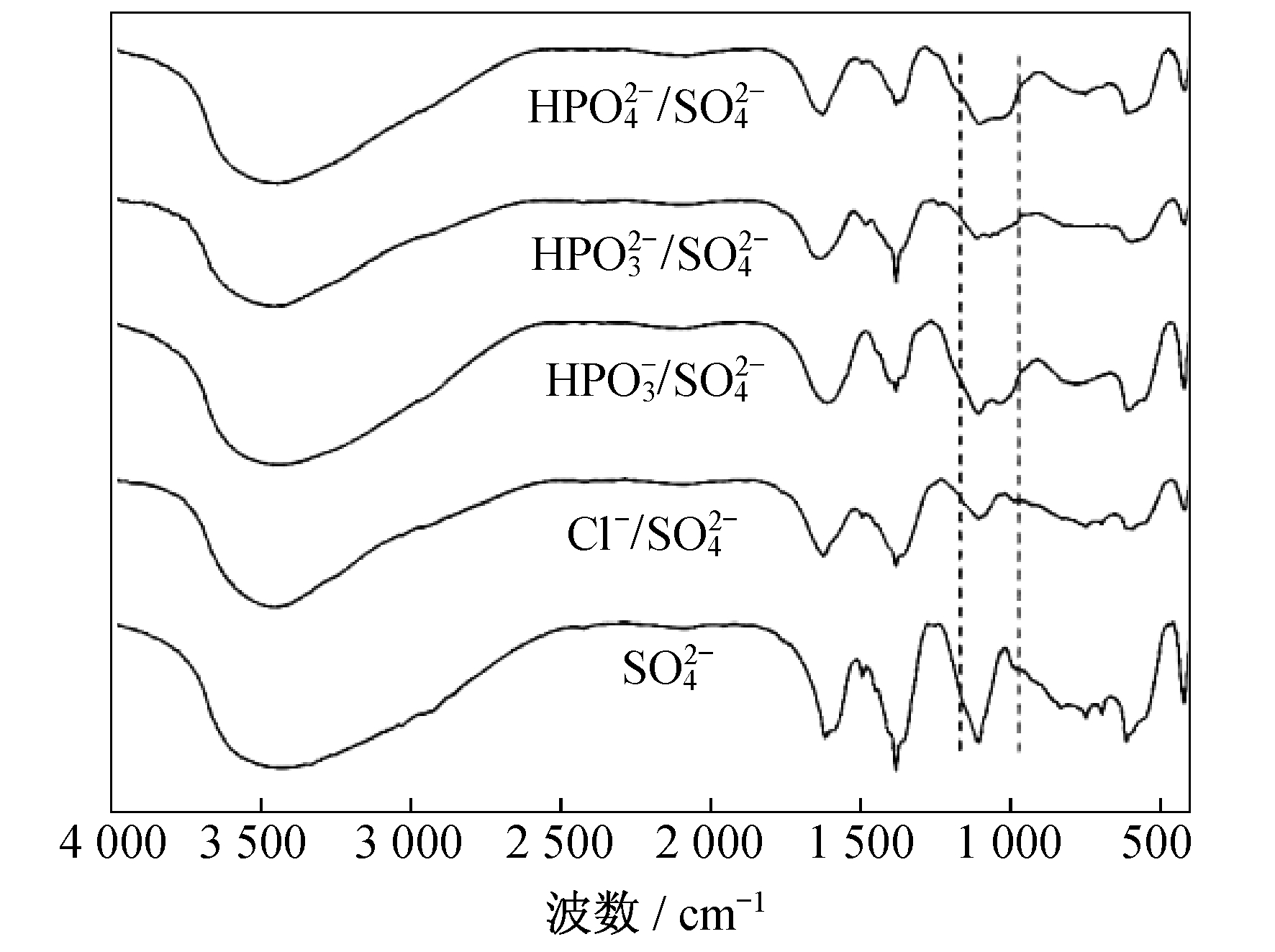
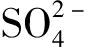 的吸收带在1 110 cm-1附近, 共存离子的存在使反应后的类水滑石复合材料FT-IR谱图中
的吸收带在1 110 cm-1附近, 共存离子的存在使反应后的类水滑石复合材料FT-IR谱图中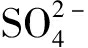 的吸收带强度减弱。当
的吸收带强度减弱。当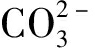 与
与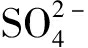 共存时,
共存时,
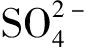 的吸收带强度最弱。通常,
的吸收带强度最弱。通常,
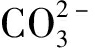 很难被替换, 因此在离子交换之前可用去除CO2预处理过的去离子水进行交换, 以增加离子交换的彻底性[
很难被替换, 因此在离子交换之前可用去除CO2预处理过的去离子水进行交换, 以增加离子交换的彻底性[

