|
|
|
发布时间: 2022-10-25 |
燃烧与污染物控制 |
|
|
|
收稿日期: 2022-04-02
基金项目: 国家自然科学基金(52076126)
中图法分类号: X773
文献标识码: A
文章编号: 2096-8299(2022)05-0427-06
|
摘要
双碳背景下, 我国能源结构将构建新的电力能源体系。在今后较长一段时期, 燃煤火电是我国能源安全的基石, 清洁低碳是发展方向, 烟气重金属排放控制是其关键研究领域。光催化、双金属硫化物脱除等重金属净化技术方兴未艾, 多种污染物协同脱除具有广阔的应用前景。
关键词
碳中和; 能源转型; 新能源体系; 能源安全; 汞砷重金属; 烟气净化
Abstract
Under the background of dual carbon, China′s energy structure will be vigorously transformed and a new power energy system will be constructed. For a long period of time in the future, coal-fired thermal power is the cornerstone of China's energy security, clean low carbon is the development direction, and heavy metal emission control of flue gas is one of the key issues. Heavy metal purification technologies such as photocatalysis and bimetal sulfide removal are in the ascendant, and the synergistic removal of multiple pollutants is the development direction with broad application prospects.
Key words
carbon neutral; energy transition; new energy system; energy security; mercury and arsenic heavy metals; flue gas purification
能源是人类社会生存的基础, 人类大约600万年前就开启了能源利用时代[1-2]。以煤、石油等为代表的高碳化石能源燃烧排放物是温室气体CO2的主要来源[3-4]。长久以来, 能源消耗产生的温室气体导致全球变暖, 生态环境形势严峻。习近平总书记在第75届联合国大会上提出了“中国二氧化碳排放力争于2030年前达到峰值、努力争取2060年前实现碳中和”的新目标。这是我国对实现社会经济发展的重大决策。然而, 2021年出现的“拉闸限电”现象, 严重影响了社会经济的健康发展。要建设社会主义现代化强国, 保障能源供应, 关键是要处理好能源与环保、短期与中长期的关系, 把“双碳”纳入经济社会发展全局, 切实做到“稳妥有序, 安全降碳”。燃煤火电是我国能源安全的基石, 但燃煤电厂发电过程中产生的SOx, NOx, 粉尘、痕量重金属元素等污染物, 严重危害了生态和谐和人类的身体健康。为了解决烟气污染问题, 各国学者对烟气污染物脱除进行了研究。汞砷等重金属排放控制是烟气深度净化的关键环节之一。近年来随着吸附、催化等技术的不断发展, 实现多种污染物协同脱除方法是烟气重金属控制的发展方向。
1 我国能源结构与烟气重金属污染排放
1.1 能源结构现状
能源是现代经济的重要支撑, 是人类社会生存和发展的重要基础[5]。工业化以来, 煤炭、石油、天然气等化石能源对经济社会发展至关重要, 但也带来了生态环境问题。20世纪80年代, 我国对火电行业的存量进行了阶段性的容量改革, “十三五”开始控制传统火力发电的增量。同时, 传统化石能源的日益短缺与社会经济发展对能源旺盛需求之间的矛盾更显尖锐, 需要优化能源结构, 加快多元化能源供给, 但煤仍是保障能源供应的基础, 是能源安全的“压舱石”。尽管与之前相比, 石油消费量急剧下降, 但在全球能源消费结构中的份额仍占比较大。2020年, 化石能源仍然在世界能源消费领域有着较高的占比, 达到了83.1%。在我国能源结构中, 2020年煤炭占比56.8%[6], 到2030年仍将保持在43%左右。
1.2 烟气中重金属排放特性
1.2.1 汞的排放特性
1.2.2 砷的排放特性
2 新能源体系构建
为推动经济社会高质量发展, 中国政府明确提出了“双碳”目标[12]。同时, 中共中央、国务院印发《关于完整准确全面贯彻新发展理念做好碳达峰碳中和工作的意见》, 系统、全局地部署“双碳”工作。《中华人民共和国国民经济和社会发展第十四个五年规划和2035年远景目标纲要》中再次提出要推进能源革命, 全面建立绿色低碳循环发展的经济体系和清洁、低碳、安全、高效的能源体系。
然而, 煤炭作为我国能源安全的基石, 在未来较长时间内, 没有资源能替代煤炭的兜底保障作用。国际数据显示, 2020年我国火电装机容量达12.45亿kWh, 占比近57%;2030年全社会用电量中, 50%来自火力发电; 2060年我国火电发电量仍可达40%以上。不可忽略的是, 未来较长一段时间能源消耗的总量仍会上升, 全社会用电量将由2017年6.4万亿kWh增长到2030年10万亿kWh。因此, 将燃煤电厂烟气重金属污染物(Hg, As, Se, Pb)排放控制在新能源体系构建、实现“双碳”目标背景下, 显得尤为重要, 也是实现可持续发展, 建立生态文明社会的应有之意。
3 烟气中重金属的控制
3.1 烟气汞的控制
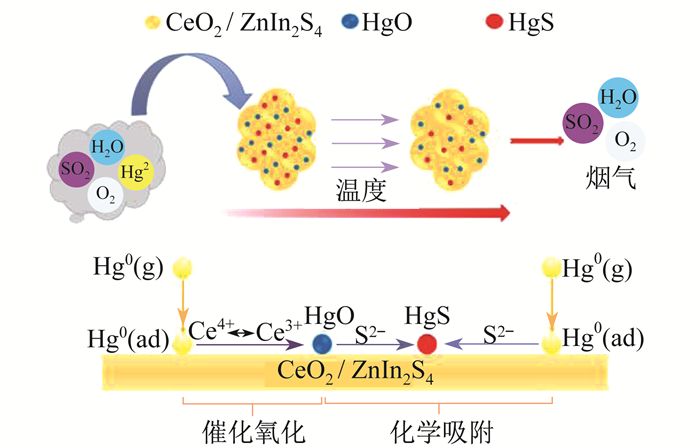
目前, 从烟气中去除Hg0的技术主要分为吸附法和催化氧化法两类。常见的吸附剂有活性炭、过渡金属氧化物、金属硫化物等。吸附技术因成本高而无法大规模应用。光催化技术作为一种新型的催化氧化方法, 可以在较宽温度窗口下运行, 是未来极具潜力的脱汞技术之一。
3.1.1 吸附法
3.1.2 催化氧化法
热催化氧化法具有低能耗、高净化效率、无二次污染等优点, 热催化剂如Pt, Pd等具有活性强、寿命长和使用稳定等优点。但大多数催化剂是贵金属, 且烟气中含有粉尘, S, Cl等有害成分, 容易造成催化剂的堵塞和中毒。催化剂的选择对操作和维护成本, 以及汞的脱除效率有很大影响。
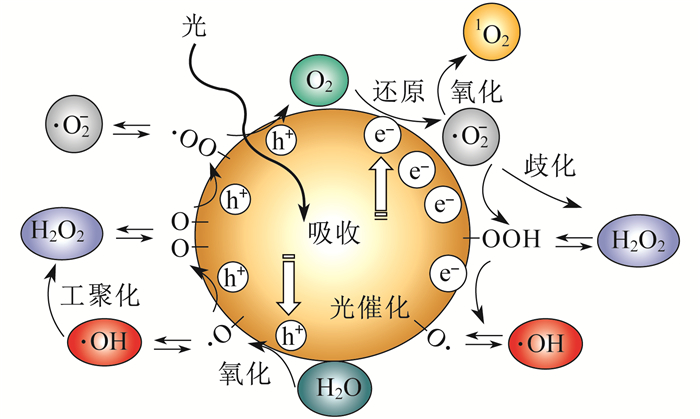
光催化技术能够将太阳能转化为化学能, 具有环境友好、节能安全、可持续发展等特点, 在解决环境污染方面具有较大的潜力[14]。光催化反应过程如图 2所示。
由图 2可知, 当光催化剂吸收能量大于禁带宽度的光子时, 其价带电子从价带跃迁至导带, 形成电子-空穴对(电荷载流子), 随后光生电子-空穴对分离, 并分别向光催化剂的表面迁移, 与吸附于光催化剂表面的水分子、氧反应生成超强活性的自由基或直接与污染物发生反应, 从而有效氧化重金属污染物[15]。
3.2 烟气砷的控制
燃煤烟气中的砷主要以三价砷的形态聚集在微粒的表面。三价砷的毒性最强, 是五价砷的50倍左右, 且在烟气中难以脱除。所以, 燃煤烟气中砷脱除技术的关键是将三价砷氧化为五价砷并固定在容易脱除的界面。吸附剂可以为砷的物理吸附提供一个可附着的表面。同时, 气态的砷化合物可以通过氧化反应在它们的活性位点上转化为稳定的砷酸盐。
根据砷在煤燃烧过程中的赋存形态和迁移特性, 可通过减少原煤中砷的含量、控制高温下产生气态砷的含量、减少亚微米颗粒上聚集砷的量等3方面进行燃煤电厂砷的减排。其中, 烟气砷脱除是重要途径。铁基吸附剂是烟气砷脱除的有效措施之一。文献[16]采用一步水热法制备了球形α-Fe2O3吸附剂进行烟气砷的吸附。结果表明: 吸附的最佳温度为600 ℃; SO2和O2对砷的吸附起到了积极的作用, 而NO对砷的吸附影响不大; α-Fe2O3吸附剂具有良好的除砷性能。α-Fe2O3的SEM图像如图 3所示。
钙基吸附剂[17]也是极具潜力的烟气砷脱除的吸附剂之一。其SME图像如图 4所示。
由图 4(a)可知, 经氧化铝改性的氧化钙(Al2O3/CaO)具有独特的片状结构和丰富的表面吸附点位; 由图 4(b)可知, 未改性的氧化钙U-CaO则有烧结聚团现象; 由图 4(c)可知, 在1 273 K温度下吸附烟气砷后, Al2O3/CaO表面发生轻微烧结现象; 由图 4(d)可知, 在1 273 K温度下, U-CaO烧结成团, 表面空隙坍塌严重。
钙基砷固定燃烧实验的结果表明, CaO对煤中砷挥发的抑制率由3.05%提高到37.35%, 平均捕集率为15.31%[18]。但钙基吸附剂的缺点也十分明显, 存在易因酸性气体的竞争吸附导致高温烧结及比表面积低等问题。针对这一问题, 文献[17]通过制备抗烧结Al2O3/CaO对烟气中As2O3进行有效脱除。结果表明, Al2O3的加入提高了CaO的抗烧结能力, Al2O3/CaO对砷的吸附能力一直保持在较高水平。
3.3 重金属控制技术的经济性分析
活性炭喷射是较为成熟的燃煤烟气汞脱除技术之一, 然而传统活性炭的吸附容量有限, 碳/汞重量比介于2 000和15 000时汞脱除率为25%~95%, 但使用活性炭实现约82%的脱汞效率时, 每千克汞的脱除成本为110 000~150 000$[19]。与昂贵的传统活性炭相比, 金属硫化物吸附剂价格低廉, 具有更高的Hg0吸附容量, 并且几乎不受烟气成分影响, 是理想的汞吸附材料。
众多固砷吸附剂中, 活性炭在低温条件下具有优异的吸附性能, 但活性炭不能直接用于吸附燃煤电厂烟气中的砷, 因为烟气温度过高会直接导致吸附剂失活, 一般最佳吸附温度为150~160 ℃。金属氧化物吸附剂中Fe2O3对砷的吸附效果最好, 其次是CaO, 最后是Al2O3。这是因为Al2O3对气相砷是物理吸附。此外, 钙基改性吸附剂以成本低、比表面积大等特点受到广泛关注, 其中对CaO的应用较为成熟, CaO/γ-Al2O3复合吸附剂的最高吸附率可达43.25%[20]。
3.4 密度泛函理论计算
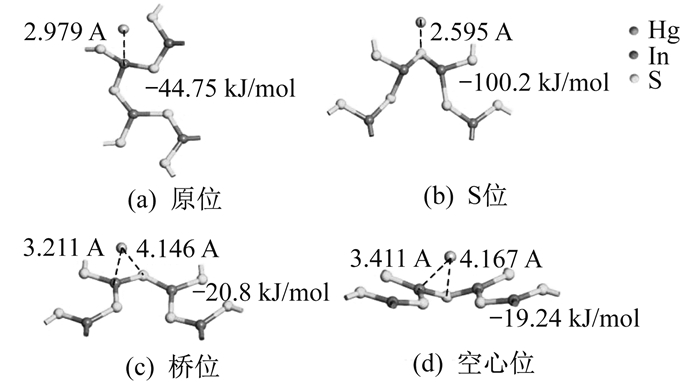
硫化物是汞脱除的重要研究方向。文献[21]计算了Hg0在In2S3表面的吸附能, 其采用广义梯度近似(GGA)方法中的Perdew-Wang 91(PW91)函数, 并应用具有轨道极化函数的双数值基(DNP), 选择In2S3(110)表面作为典型表面进行计算。图 5显示了In2S3(110)表面汞的4种可能的稳定吸附构型(原位、S位、桥位和空心位)。由图 5可知, 原位、S位、桥位和空心位的吸附能分别为-44.75 kJ/mol, -100.2 kJ/mol, -20.8 kJ/mol, -19.24 kJ/mol, 其中S位是最稳定的吸附位。计算结果表明, S原子与Hg0之间存在很强的亲和力, S位是主要的活性位。
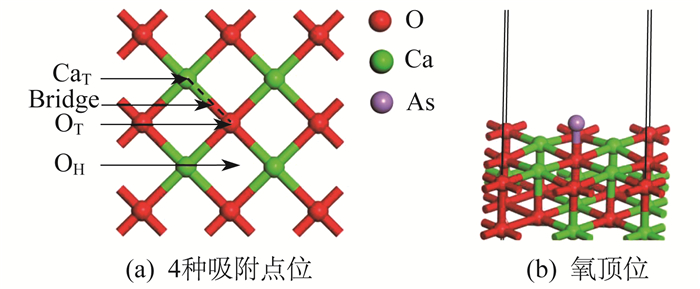
钙基吸附剂吸附法是重要的烟气砷吸附脱除方法。文献[17]运用密度泛函理论, 采用计算模拟对此进行了研究。CaO(001)4种吸附位点和As在OT的吸附模型如图 6所示。
由图 6(a)可知, As在CaO(001)上的吸附位置主要有氧顶位(OT)、钙顶位(CaT)、氧空位(OH)、桥位(Bridge)。通过将As在CaO(001)不同位点上进行优化, 确定CaO(001)的主要吸附活性位点, 得到的吸附能、键长等参数。As在氧顶位的优化结果如图 6(b)所示。
模型经过优化后, 得到了As在CaO(001)吸附后的结构参数, 如表 1所示。
表 1
As在CaO(001)吸附后的结构参数
| 吸附位点 | 吸附能/(kJ·mol-1) | 键长/nm |
| OT | -374.96 | As-O: 0.192 1 |
| CaT | -124.56 | As-Ca: 0.290 1 |
| Bridge | -341.51 | As-O: 0.189 7 |
| As-Ca: 0.311 4 | ||
| OH | -133.51 | As-O: 0.258 1 |
| As-Ca: 0.274 3 |
由表 1可以发现, As在氧顶位上的吸附能最高, 达到-374.96 kJ/mol, 而在钙顶位仅达到-124.56 kJ/mol, 并且在氧顶位的As-O键长缩小到0.192 1 nm, 因此氧顶位是CaO吸附As的主要活性点位。
3.5 多污染协同控制
如前所述, 燃煤发电拥有巨大电力供给优势, 同时, 燃煤烟气排放SO2, NOx, 汞、砷等重金属污染物对环境造成危害[21]。各国学者对单一污染物的脱除进行了不同的研究, 但由于不同污染物脱除所需的氧化还原环境相矛盾, 因此燃煤电厂污染物的协同控制仍然面临挑战[22]。
不同的烟气组分通常会对脱汞性能产生不同的影响。一般情况下, 烟气中NO的存在能提高Hg0转化为Hg2+的转化率。这是因为NO可以转化为NOx或NO+等活性物质, 促进汞的吸附。然而, SO2对汞的吸附具有双重影响: 一方面, SO2会与Hg0竞争吸附活性位点, 从而降低吸附效率。另一方面, 当O2存在时, 烟气中SO2被氧化为SO3, SO3与H2O生成H2SO4, H2SO4可将Hg0氧化为HgSO4。这将有利于汞的吸附。
在汞、砷等重金属与氮氧化物(主要为NO)、二氧化硫协同脱除方面可采取以下方法和措施。
(1) 采用SCR脱硝催化剂将NO氧化为NO2的同时, 可以将烟气中的Hg0氧化为Hg2+。对于砷来说, 将As3+氧化为As5+, 所得的氧化产物NO2和Hg2+(或As5+)均有亲水性, 可以在脱硫塔中协同去除。即利用脱硫塔实现NO、重金属汞或砷及SO2协同脱除的效果。
(2) 制备具有光催化氧化-吸附一体化性能的新型光催化剂, 将其放置在烟囱的适当位置, 达到光催化氧化吸附一体化的效果。
(3) 在电厂现有的大气污染控制设备, 静电除尘器的前端喷射吸附/催化剂, 吸附重金属, 然后采用电除尘或布袋除尘法, 将吸附有重金属的吸附/催化剂与飞灰一同捕捉下来, 从而实现多污染系统协同脱除。
4 结语
“双碳”目标的提出是以煤电为主的我国能源结构的深层次的构建与变革, 需要加快能源领域技术突破和创新, 打造清洁高效现代能源体系, 推动能源低碳转型平稳过渡是发展方向。燃煤火电是新能源体系构建的安全基石, 清洁低碳是必由之路。
烟气汞、砷重金属排放控制是烟气深度净化的关键环节。传统活性炭技术相对成熟但成本高。硫化物脱汞是重要的研究方向之一, 近年来快速发展的光催化技术是未来极具潜力的Hg0脱除技术; 改性钙基吸附剂吸附法是烟气砷脱除的重要技术路径; 多种污染物协同脱除是烟气重金属控制的未来发展方向。
参考文献
-
[1]WEEKES-SHACKELFORD V, SHACKELFORD T K, WEEKESSHACKELFORD V A. Encyclopedia of evolutionary psychological science[M]. Cham: Springer International Publishing, 2016: 1-4.
-
[2]SENUT B, PICKFORD M, GOMMERY D, et al. First hominid from the Miocene[J]. Earth and Planetary Science, 2001, 332(2): 137-144.
-
[3]YAO L, GARMASH O, BIANCHI F, et al. Atmospheric new particle formation from sulfuric acid and amines in a Chinese megacity[J]. Science, 2018, 361: 278. DOI:10.1126/science.aao4839
-
[4]HUANG R J, ZHANG Y L, BOZZETTI C, et al. High secondary aerosol contribution to particulate pollution during haze events in China[J]. Nature, 2014, 514(12): 218-222.
-
[5]张海龙. 中国新能源发展研究[D]. 长春: 吉林大学, 2014.
-
[6]张所续, 马伯永. 世界能源发展趋势与中国能源未来发展方向[J]. 中国国土资源经济, 2019, 32(10): 20-27.
-
[7]CHEN B, WANG X B, LI Y L, et al. Energy-induced mercury emissions in global supply chain networks: Structural characteristics and policy implications[J]. Science of the Total Environment, 2019, 670: 87-97. DOI:10.1016/j.scitotenv.2019.03.215
-
[8]胡长兴, 周劲松, 何胜, 等. 静电除尘器和湿法烟气脱硫装置对烟气汞形态的影响与控制[J]. 动力工程, 2009, 29(4): 5.
-
[9]BUNT J R, WAANDERS F B. Trace elementbehaviour in the Sasol-Lurgi MK IV FBDB gasifier[J]. Fuel, 2008, 87(12): 74-87.
-
[10]赵峰华, 任德贻, 彭苏萍, 等. 煤中砷的赋存状态[J]. 地球科学进展, 2003, 18(2): 214-220. DOI:10.3321/j.issn:1001-8166.2003.02.010
-
[11]TIAN H, WANG Y, XUE Z, et al. Atmospheric emissions estimation of Hg, As, and Se[J]. Science of the Total Environment, 2011, 16: 3078-3081.
-
[12]SONG B, SONG M, CHEN D, et al. Retention of arsenic in coal combustion flue gas at high temperature in the presence of CaO[J]. Fuel, 2020, 259(1): 116249.
-
[13]TAO J, ZHENG J C, JIANG W, et al. Nanosized ZnIn2S4 supported on facet-engineered CeO2 nanorods for efficient gaseous elemental mercury immobilization[J]. Journal of Hazardous Materials, 2021, 416: 126436.
-
[14]XY C, ANUSUYADEVI P R, AYMONIER C, et al. Nanostructured materials for photocatalysis[J]. Chemical Society Reviews, 2019, 48(14): 3868-3902.
-
[15]NOSAKA Y, NOSAKA A Y. Generation and detection of reactive oxygen species in photocatalysis[J]. Chemical Reviews, 2017, 117(17): 11302-11336.
-
[16]PENG C Z, JIAN G, QIAN Y L, et al. Microscopic spherical α-Fe2O3 for highly efficient gaseous arsenic capture in simulated flue gas under a wide temperature range[J]. Energy Fuels, 2021, 35(23): 19581-19591.
-
[17]HONG J, ZHAO Y, WU J, et al. Fabrication of Al2O3/CaO with anti-sintering for efficient removal of As2O3 in simulated flue gas: experimental and DFT study[J]. Fuel, 2022, 307(1): 121812.
-
[18]张军营, 任德贻, 钟秦, 等. CaO对煤中砷挥发性的抑制作用[J]. 燃料化学学报, 2000(3): 7-9.
-
[19]LOPEZ A M A, FERNANDEZ-M N, MARTINEZ T M R. The application of regenerable sorbents for mercury capture in gas phase[J]. Environmental Science Pollution Research, 2016, 23: 24495-24503.
-
[20]陈锦凤. CaO/γ-Al2O3干法脱除燃煤烟气中砷的实验研究[J]. 华中师范大学学报(自然科学版), 2013, 47(4): 519-522.
-
[21]ZHOU M, XIE X, LIU Q, et al. Spherical In2S3 anchored on g-C3N4 nanosheets for efficient elemental mercury removal in the wide temperature range[J]. Chemical Engineering Journal, 2022, 430: 132857.
-
[22]章玲, 潘卫国, 吴江, 等. 燃煤电站锅炉多种污染物联合脱除技术的比较与分析[J]. 上海电力学院学报, 2010, 26(4): 322-326.